지난 9월 21일(현지시각) 스위스 로잔 연방공대(EPFL)와 미국 캘리포니아대로스앤젤리스(UCLA), 하버드대 공동 연구팀이 유전자치료를 통해서 척수 손상으로 인해 하반신이 마비된 쥐를 회복시켰다는 연구결과가 나왔다. 척수는 척추 중추신경계를 의미한다.
이번 기술은 그 자체로 마비에 대한 근본적인 치료방법을 알아냈다는 평가를 받고 있기에 어떤 기술인지, 원리는 무엇인지 등 여러가지 측면에 대해서 의생명공학과를 재학 중인 필자의 시각으로 설명하려 한다.
이번 발견이 획기적인 이유
예전부터 신경을 재생시키는 등의 연구는 활발히 이루어졌었고, 사실 하반신 마비의 원인이 되는 척수의 신경세포 자체를 재생시키는 기술은 2018년에 개발이 되어있었다. 그리고 작년, 인공신경세포를 통해서 하반신 마비인 쥐가 뛰기까지 했다.
그렇다면 이번 연구결과가 각광받는 이유는 무엇일까? 이전 기술에서는 신경세포를 재생시켜도 하반신 마비의 치료로는 이어지지 않았고, 인공신경의 경우 전력을 통한 움직임 조절이 필요했다. 즉, 전기 등 외부의 개입이 어느정도 필요하단 것이다. 하지만 이번 발견은 신경세포를 올바른 곳에 위치시키는 성장인자의 발견을 통해서 이뤄진 것으로, 외부의 개입 없이 신경세포를 재생, 연결시킬 수 있다.
즉, 이번 발견은 신경손상을 복구하는 근본적인 치료법을 발견한 셈이기에 의미가 있다. 위에서 기술한 것처럼 전부터 신경손상의 경우 재생은 가능해도 한번 손상되고 퇴행이 시작된 신경은 다시 회복되기 어렵다.
그렇기에 연구자들은 인공신경을 만들고 이식하거나 전기 자극을 통해서 신경의 작용방식을 모방하는 것같이 신경손상을 공학적인 방식으로 접근하고 있었다. 그러나 이번 발견을 통해서 신경손상에 대한 생물학적, 의학적 방식의 치료의 실마리인 성장인자의 존재를 알려주었기에 이와 관련된 연구가 더욱 발전할 거라 전망된다는 점에서 이번 연구 결과가 주목받고 있다.
신경세포 재생의 원리
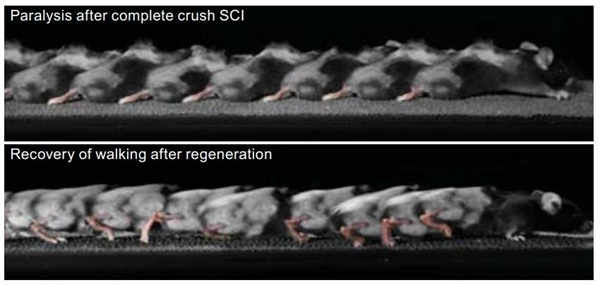
▲하반신마비 쥐(위) 와 유전자치료 쥐(아래) 의 걷는모습 차이 ⓒ science지
신경세포(뉴런)에는 신경전달물질을 받는 가지돌기와 신경전달물질을 전달하는 축삭돌기가 있다. 하반신 마비의 경우 신경세포가 손상되고 끊어져서 신경전달물질이 다음 신경세포로 전해지지 않는 것이라 할 수 있다. 이에 연구팀은 경미한 신경손상을 입은 쥐의 자연회복과정을 추적해서 척수 속 신경세포를 분석하여 원리를 알아내기 위해 노력한 결과 특정 성장인자의 존재를 알게 되었다.
성장인자는 세포의 증식, 상처 치유 세포 분화를 자극할 수 있는 자연 발생 물질로 일반적으로 단백질 또는 스테로이드 호르몬이다. 이러한 성장호르몬은 세포사이의 신호분자로 작용하는데, 연구진이 신경세포를 올바르게 연결되도록 하는 신호를 만들어내는 성장인자를 발견한 것이다.
다시 말해, 이전까지는 신경세포가 재생되어도 척수까지 이어지지 않았지만, 이번 연구결과인 성장인자를 통해서 신경세포를 올바른 위치에 연결시켜 마비가 왔던 부위에 신경전달물질이 바르게 전달될 수 있게 되는 것이다.
마비를 정복할 수도 있을까
먼저 말하기에 앞서서 필자는 현재 의생명공학과를 재학중인 대학생이다. 그렇기에 의생명공학과가 보기에 어떻게 기술이 발전하거나 융합될지에 대해 말해보려 한다.
이번 연구는 척수에 있는 뉴런 자체를 올바르게 재생, 연결시킬 수 있는 방법을 찾은 것이기 때문에, 향후 올바른 성장인자를 찾을 수만 있다면 거의 모든 신경손상에도 적용이 가능할 것이라 예측한다.
예를 들어 교통사고로 인한 마비증세가 있다. 이전에도 교통사고로 인해 하반신이 마비된 남성이 척수에 전극을 이식받고 다시 걷게 된 연구결과가 있는데, 이와 비슷하게 이번 기술이 사람에게 적용될 수 있게 된다면 교통사고로 인해 오는 하반신, 혹은 전신마비를 정복할 가능성도 있는 것이다.

▲휠체어(자료사진). ⓒ pixabay
또한 기술의 활용 측면에서 본다면, 전기자극치료법을 통해서 뉴런을 회복시킨 이후 재활을 전기자극을 통해 돕는 등 기술들 간의 단점을 상쇄하거나, 치료에 걸리는 기간을 단축시키는 방향으로 기술이 융합될 가능성이 높다.
한편 신경질환이라 하면 아마 대부분이 치매, 알츠하이머를 먼저 떠올릴 거라고 생각한다. 그렇다면 신경을 재생시키고 연결시키는 이번 기술이 알츠하이머와 관계가 있을까? 이를 말하기 전에 알츠하이머에 대해 알아보자.
알츠하이머는 뇌의 신경세포에서 아밀로이드 베타와 타우라는 특정 단백질이 과하게 생성되고 엉킨 채로 뇌 속에 축적되어서 생기는 질병이다. 원리가 정확히 알려진 건 아니지만, 학계에선 타우 단백질이 엉킨 채로 축적된 후 노후 단백질을 세포에서 제거하는 자가 포식 기능이 노화되고 둔화되기 때문으로 추정하고 있다. 여기서 알 수 있듯이 신경퇴행성질환은 뉴런 자체만의 문제가 아니기에 이번 기술 자체만으로 해결하기엔 갈 길이 남았다고 할 수 있다.
인간에게도 적용할 수 있을까
이번 실험이 실험용 쥐를 대상으로 진행된 만큼, 차후 인간에겐 적용이 가능한지도 궁금해진다. 아직 동물 실험일 뿐이기에 당연히 '쥐랑 인간은 다르지 않느냐?' 라는 의문을 제기할 수 있다.
그러나 대부분의 경우 동물실험의 결과는 인간의 경우를 꽤 잘 예측하는 편이다. 오히려 인공 배양 조직이나 시뮬레이션처럼 일부에서만 활성이 있던 인자들이 유기체 속에서 기능을 못하는 경우가 더 허다하다.
생물의 개체 단위에서의 생명활동은 매우 복잡하고 하나의 단백질이 여러가지 역할을 하듯이 시뮬레이션, 혹은 인공 배양 조직으로는 예측할 수 없는 변수들이 생물속에 존재한다. 그렇기에 실험용 쥐를 통한 실험은 유기체의 활동을 모두 포함하는 실험결과를 도출한다. 따라서 인간에게도 꽤나 높은 적중률을 보일 수 있는 것이다.
그렇다면 인간에겐 어떤 식으로 적용이 가능할까? 향후 인간에게도 신경세포를 올바르게 위치시키고 척수에 연결시켜주는 성장인자를 찾으면 될 것이라 생각한다. 다만, 경미하게 신경이 손상된 인간을 대상으로 생체실험을 할 수 없으므로 신경을 회복하는 단계에서 어떤 인자들이 개입하는지 알아내는 과정, 즉 성장인자를 어떤 과정을 통해서 알아낼 수 있을지 정하는 것이 중요하다고 생각한다.
성장 인자를 발견했다는 연구결과는 손상 입은 신경세포 자체를 재생시키고, 올바르게 연결시켜 운동능력을 회복하는 것이기에 올바른 방향으로 활용, 개발된다면 척수와 같은 신경 뿐 아니라 시신경이나 치아 쪽의 신경과 같은 다른 여러 신경세포들에게도 적용 가능해 질 것이라 생각한다. 앞으로의 연구가 더 기대되는 이유다.