▲페로토시스 유도제(RSL3)와 다라플라딥(포스포라이페이스 A2)를 함께 사용했을 때의 위암 세포사멸 효과. 2종의 위암 세포주(Hs746T, SNU-484)에 페로토시스 유도제(RSL3)와 다라플라딥(포스포라이페이스 억제제)을 함께 사용한 경우, RSL3를 단독 사용한 경우보다 위암 세포의 사멸이 크게 증가함.
한국생명공학연구원 제공
전체 암 발생 4위에 해당하는 '위암' 치료 해법으로, 페로토시스(Ferroptosis) 지방 대사 조절 메커니즘과 다라플라딥(Darapladib) 약물 재창출을 통한 새로운 '난치성 항암 치료 물질'을 국내 연구진이 발굴해냈다.
한국생명공학연구원(원장 김장성, 아래 생명연) 이은우‧한백수 박사, 한국기초과학지원연구원(원장 양성광, 아래 기초지원연) 황금숙 박사 공동 연구팀은 21일 "지방 대사를 조절하는 메커니즘을 활용해 난치성 위암의 새로운 치료 물질을 개발하는 데 성공했다"고 밝혔다.
위암의 경우 2022년 발표된 중앙암등록본부 자료에 의하면 '2020년 전체 암 발생의 4위(10.8%)'에 해당하며 여전히 상위권을 차지하고 있다. 이런 상황에서 이번 치료 물질 개발은 항암 내성 위암을 비롯한 다양한 난치성 암 치료에 대안이 될 것으로 기대가 모아지고 있다.
연구팀은 "여러 항암제의 개발에도 여전히 위암은 약물로 치료하기 어려워 수술이 우선시 되고 있다"면서 "특히 암이 위의 점막하층을 지나 근육층 이상을 뚫고 들어간 진행성 위암의 경우 효과적인 치료제가 없는 상황"이라고 짚었다.
이는 '진행성 위암'이 쉽게 전이되는 특성과 함께 기존 항암제에 내성을 가지며 재발하기 때문이며, 이를 해결하기 위한 연구가 다양하게 진행되고 있지만 여전히 많은 연구를 필요로 하고 있다. 최근에는 '페로토시스(Ferroptosis)'가 항암제 내성암을 비롯한 여러 난치성 암을 사멸시키는 새로운 경로로 주목받고 있다고 한다.
연구팀은 "페로토시스는 세포 내 철분이 과도하게 축적되면 세포막을 구성하는 인지방질(phospholipid)이 활성산소에 의해 과산화(peroxidation)되어 세포 내 물질에 영향을 미치고, 이는 세포막과 미토콘드리아에 손상을 입혀 세포가 죽음을 맞이하게 되는 과정을 말한다"고 설명했다.
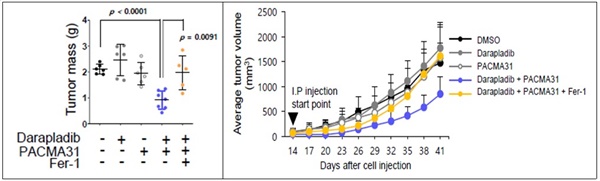
▲실험동물 대상 페로토시스 유도제(PACMA31)와 다라플라딥(포스포라이페이스 A2)를 함께 사용했을 때의 종양 사멸 효과. 면역을 결핍시킨 쥐의 복강에 다라플라딥(포스포라이페이스 억제제)와 페로토시스 유도제(PACMA31)를 함께 투여한 결과 종양의 크기와 부피가 크게 감소함.
한국생명공학연구원 제공
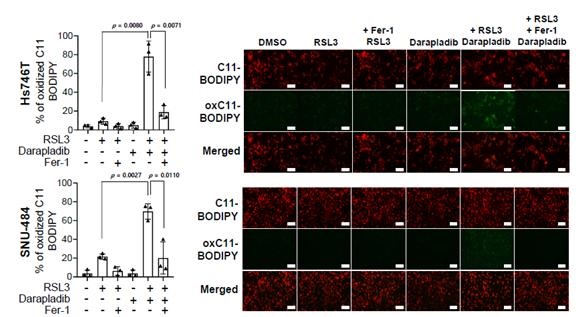
▲페로토시스 유도제(RSL3)와 다라플라딥(포스포라이페이스 A2)을 함께 사용했을 때의 지질 과산화 정도 측정. 2종의 위암 세포주(Hs746T, SNU-484)에 페로토시스 유도제(RSL3)와 다라플라딥(포스포라이페이스 억제제)을 함께 사용한 경우, 페로토시스의 주요 특징인 지질 과산화 정도가 크게 증가함.
한국생명공학연구원 제공
이에 연구팀은 탁월한 세포사멸에 기전을 가진 '페로토시스'를 항암치료제로 이용하기 위해 페로토시스 유도제와 403개의 대사 약물을 혼합하며 최적의 조합을 찾기 위한 연구를 거듭했다고 한다.
그 결과, 페로토시스 유도제와 포스포라이페이스 A2(Phospholipase A2, 인지질 가수분해효소 A2) 억제제의 조합이 항암제 내성암을 비롯한 여러 암을 효과적으로 사멸할 수 있음을 밝혀낼 수 있었다.
특히 연구팀은 페로토시스 유도제 RSL3(RAS-selective lethal 3, RAS 선택적 치사 3)와 다라플라딥(Darapladib)을 함께 사용했을 때 탁월한 사멸 효과가 나타나는 것을 확인했다.
'다라플라딥'은 혈관에 지방질이 들러붙는 것을 줄일 수 있다고 알려져 동맥경화증 치료를 위해 개발되었다 중단된 신약후보 물질이라고 한다. 이 다라플라딥이 산화된 인지질인 PE를 리소포스파티딜에탄올아민(lysoPE, lysophosphatidyl ethanolamine)과 유리 지방산(FFA, free fatty acid)으로 분해되는 것을 억제하여 페로토시스가 촉진되는 것을 연구팀이 밝혀낸 것이다.

▲연구책임자 이은우 박사.
한국생명공학연구원 제공
연구책임자인 이은우 생명연 박사는 "이번 연구는 출연연 간 협력 연구를 통해 세포의 지방질 재편성 경로를 밝혀 새로운 항암치료 전략을 제시한 것"이라며 "특히 관상동맥질환에 대한 임상 3상에서 실패한 다라플라딥과 같이 이미 허가받지 못한 후보물질을 재창출할 수 있는 가능성이 열렸다"고 강조했다.
공동 연구책임자인 황금숙 기초지원연 박사는 "암세포의 빠른 지질 재편성 경로 규명에 활용된 질량분석기 기반의 지질체 분석 및 대사추적 신기술은 앞으로 난치성 질환의 새로운 치료 타겟 발굴에 핵심적인 역할을 할 것"이라고 전했다.
한편 이번 연구는 NST 창의형융합연구사업과 과학기술정보통신부(장관 이종호) 원천기술개발사업 및 과학기술분야 기초연구사업, 생명연 주요사업, 기초지원연 주요사업의 지원으로 수행됐다. 연구 결과는 지난 9월 15일 세계적인 과학저널인 <Nature Communications (IF 16.6)> 온라인 판에 게재됐다.

▲교신저자 한백수 박사(두 번째 줄 왼쪽부터 두 번째), 제1저자 오미희 박사(첫 번째 줄 왼쪽부터 첫 번째), 공동 제1저자 이지윤 박사(첫 번째 줄 왼쪽부터 두 번째)
한국생명공학연구원 제공
저작권자(c) 오마이뉴스(시민기자), 무단 전재 및 재배포 금지
오탈자 신고
용산 대통령실 마감하고, 서울을 떠나 세종에 둥지를 틀었습니다. 진실 너머 저편으로...
공유하기
'난치성 위암' 치료 길 열리나... 새 항암 치료물질 발굴
기사를 스크랩했습니다.
스크랩 페이지로 이동 하시겠습니까?
연도별 콘텐츠 보기