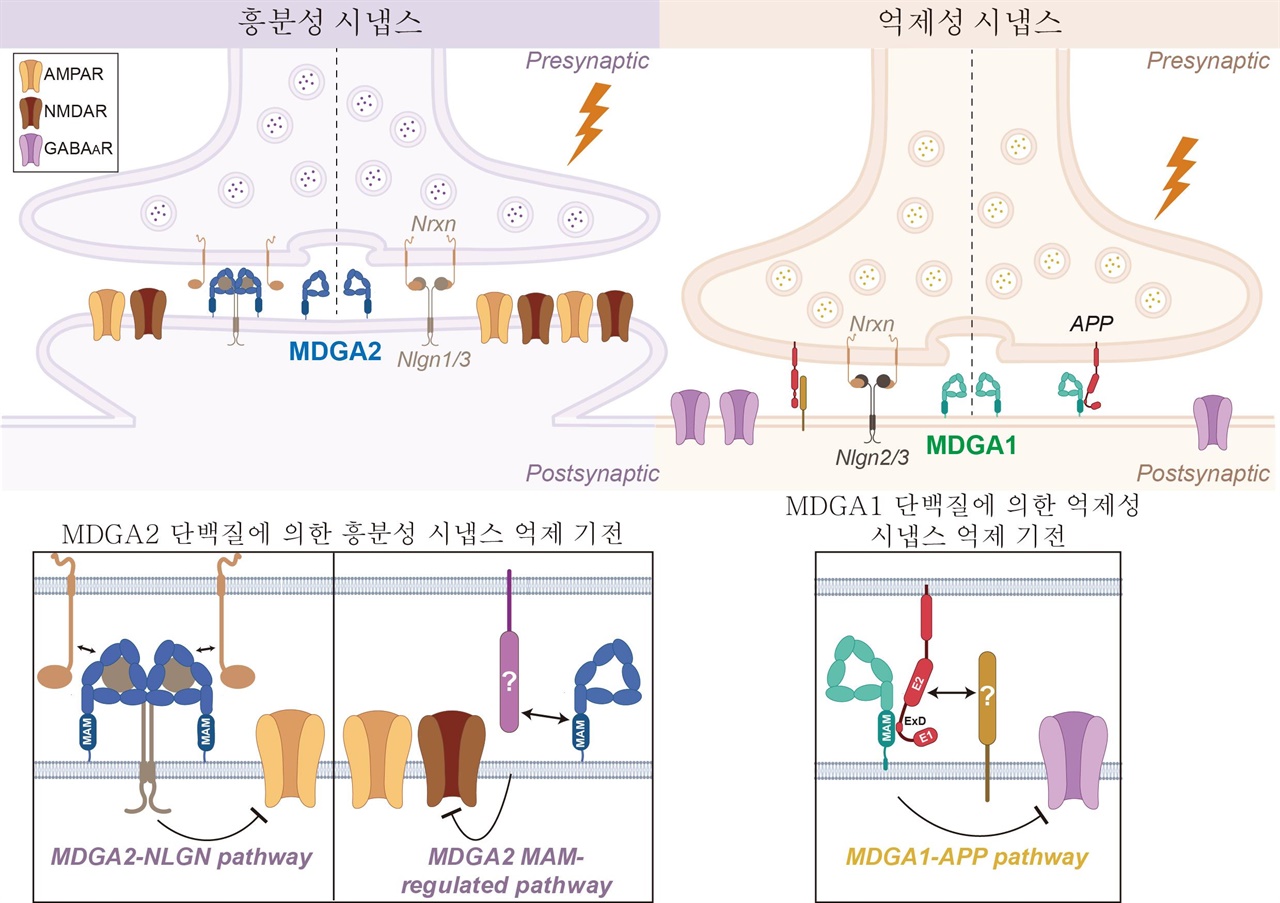
▲MDGA1은 억제성, MDGA2는 흥분성 시냅스에서 특이적으로 작용하여 서로 다른 분자기전들을 통해 시냅스 신호전달 및 시냅스 강도를 음성적으로 조절하는 인자임. 흥분성 시냅스 (왼쪽)에서는 MDGA2는 neuroligin 단백질 경로를 방해하여 AMPA 수용체 기능을 조절하고 추가로 MAM 도메인 기전을 방해하여 NMDA 수용체 기능을 방해한다. 억제성 시냅스에서는 MDGA1은 MAM 도메인 기전을 특이적으로 방해하여 GABAA 수용체 기능을 방해한다. APP 단백질이 어떻게 억제성 시냅스 조직화에 기여하는지에 대해서는 아직까지 명확하지 않음. ⓒ DGIST 제공
신경세포 연결의 숨은 지휘자로 불리는 MDGA(MAM domain containing glycosylphosphatidylinositol anchor : 신경세포가 서로 연결되어 신경 신호를 전달하는 과정에서 필수정 역할을 하는 시냅스 접착 단백질)의 비밀이 밝혀졌다.
이로써 MDGA 단백질에 의해 억제되는 다양한 시냅스 단백질 복합체를 대상으로 한 관련 뇌질환 치료제 개발에 핵심 단서 제공할 것으로 기대된다.
DGIST(대구경북과학기술원, 총장 이건우) 뇌과학과 시냅스 다양성 및 특이성 조절 연구단(센터장 고재원)은 24일 "뇌의 신경세포 연결 부위인 시냅스의 다양한 특성을 조절하는 단백질의 작동 원리를 밝혀냈다"면서 "신경회로 내 특정 시냅스 특성을 정교하게 조율해 뇌 질환 치료제 개발에도 활용될 수 있을 것으로 기대된다"고 밝혔다.
시냅스(Synapse : 신경세포접합부(神經細胞接合部))는 신경세포(뉴런)들이 서로 연결되는 특별한 지점으로, 모든 뇌 기능을 가능하게 하는 기본단위이다. 다양한 시냅스 접착 단백질은 이 연결 지점에서 신경 신호를 빠르고 정확하게 전달하여 신경회로의 특성을 결정한다.
DGIST에 따르면, 고재원 교수 연구팀(시냅스 다양성 및 특이성 조절 연구단)은 2011년부터 다양한 시냅스 접착 단백질을 연구해왔다. 특히 2013년에는 'MDGA단백질이 시냅스 구조와 신경 신호 전달을 억제하는 역할을 한다'고 규명했고, 2017년에는 이 단백질의 구조와 작동 모델을 제시했다. 그러나 이후 다른 연구팀들이 상반된 결과를 보고하면서 MDGA 단백질의 정확한 기능에 대해 의문이 제기됐었다고 한다.
이런 가운데 고 교수 연구팀은 이번 본 연구에서 특정 시간에 특정 조직에서 유전자가 삭제되도록 조작한(조건부 낙아웃) 생쥐 모델을 사용해, MDGA 단백질이 신경세포에서 어떤 역할을 하는지 조사했다. 연구팀은 공초점 현미경과 전기생리학 기법을 활용했으며, MDGA 단백질이 흥분성 및 억제성 시냅스에 미치는 영향을 분석했다.
연구팀은 "그 결과, MDGA1 단백질이 삭제되면 억제성 시냅스의 숫자와 강도가 증가하고, MDGA2 단백질이 삭제되면 흥분성 시냅스의 특성이 증가하는 것을 발견했다"면서 "이는 MDGA 단백질이 시냅스에서 특이적으로 작용한다는 것을 보여준다"고 강조했다.
이어 "다른 연구팀들은 MDGA 단백질을 연구할 때 조건부 낙아웃 모형이 아닌 다른 유전자 조작법을 사용했기 때문에 해석에 어려움이 있었다"면서 "그러나 이번 연구는 신경 세포 외의 MDGA 단백질 기능을 배제하고, 정교한 유전자 삭제 생쥐 모델을 사용하여 MDGA 단백질의 정확한 기능을 밝혀냈다"고 설명했다.
무엇보다도 연구팀은 MDGA1과 MDGA2 단백질이 서로 다른 방식으로 시냅스를 조절한다는 것을 확인했다. 놀랍게도 두 단백질을 동시에 삭제하면 시냅스 특성 변화가 사라졌는데, 이는 두 단백질이 흥분성 시냅스와 억제성 시냅스 간의 상호작용에 관여한다는 것을 보여줬다.
고재원 연구단장은 "이번 연구는 그동안 여러 논란이 많았던 MDGA 단백질의 기능을 조건부 낙아웃 생쥐모델을 이용하여 체계적으로 분석한 최초의 논문"이라며 "현재 신경세포 외의 세포들에서의 MDGA 단백질 기능을 연구 중"이라고 말했다.
한편, 이번 연구는 과학기술정보통신부와 한국연구재단의 '리더연구사업', '중견연구사업', '세종과학펠로우쉽' 등의 지원을 받아 수행됐으며, 연구 성과는 국제 전문학술지 <미국국립과학원회보(Proceedings of The National Academy of Sciences of the United States of America)>(영향력 지수: 11.1)에 6월 21일자로 온라인 게재됐다.

▲사진 왼쪽부터 DGIST 뇌과학과 시냅스 다양성 및 특이성 조절 연구단 소속 김승준 박사(DGIST 뇌과학과 석박통합과정 졸업, 공동 제1저자), 장규빈 연구원(DGIST 뇌과학과 석사과정 졸업, 공동 제1저자), 고재원 교수. ⓒ DGIST 제공